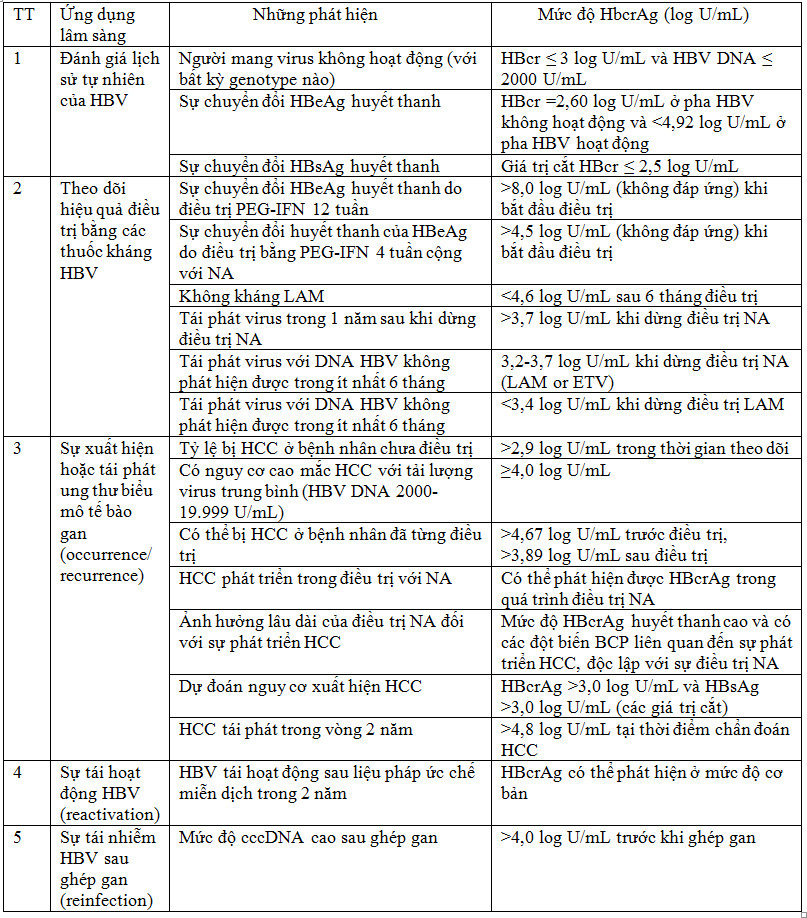
RNA tiền gen của virus viêm gan B (HBV pgRNA): một dấu ấn mới cho hoạt động của cccDNA trong gan ở bệnh nhân viêm gan B mạn
Nguyễn Nghiêm Luật
Bệnh viện Đa khoa MEDLATEC
Tóm tắt
1) HBV RNA tiền gen (pgRNA) là sản phẩm phiên mã trực tiếp của DNA vòng kín cộng hóa trị (cccDNA) của virus viêm gan B, đóng vai trò quan trọng trong quá trình khuếch đại và sao chép bộ gen của virus. Khác với HBsAg huyết thanh, pgRNA huyết thanh 3,5 kb chỉ được sản xuất từ cccDNA, do đó, nó có thể phản ánh chính xác chính xác tình trạng phiên mã của HBV cccDNA trong nhân tế bào gan.
2) Sử dụng: HBV pgRNA có thể được sử dụng để dự đoán các giai đoạn lịch sử tự nhiên của viêm gan B mạn (CHB), đánh giá đáp ứng với điều trị với PEG-IFN hoặc với các chất tương tự nucleos(t)ide (NAs), khả năng chuyển đổi huyết thanh của HBeAg, dự đoán sự tái hoạt động của HBV và thời điểm thích hợp để tạm ngừng điều trị kháng virus.
3) Chỉ định: HBV pgRNA có thể được chỉ định để dự đoán các giai đoạn lịch sử tự nhiên của viêm gan B mạn (CHB), đánh giá đáp ứng với điều trị PEG-IFN hoặc các chất tương tự nucleos(t)ide (NAs), sự chuyển đổi huyết thanh của HBeAg, dự đoán sự tái hoạt động của HBV và thời điểm thích hợp để tạm ngừng điều trị kháng virus.
4) Nồng độ pgRNA của HBV huyết thanh được đo bằng phương pháp qPCR định lượng thời gian thực với phạm vi tuyến tính của plasmid tiêu chuẩn là ∼1×101 đến 1×103 copies/mL và giới hạn phát hiện là 1×103 copies/mL. HBV PgRNA huyết thanh có thể được phát hiện ngay cả khi mức độ HBV DNA trong huyết thanh dưới 20 IU/mL.
5) Ý nghĩa lâm sàng của HBV pgRNA:
• HBV pgRNA huyết thanh có thể hoạt động như một dấu ấn sinh học để dự đoán các giai đoạn của lịch sử tự nhiên ở bệnh nhân viêm gan B. Nồng độ pgRNA của HBV trong huyết thanh thấp hơn rõ rệt ở những bệnh nhân HBeAg âm tính so với ở những bệnh nhân HBeAg dương tính, với nồng độ thấp nhất ở những người mang virus không hoạt động.
• Trong quá trình điều trị bằng peginterferon alfa-2a ở bệnh nhân CHB, nồng độ pgRNA của HBV ở tuần điều trị 12 và 24 (lần lượt là ≤5,47 và ≤5,46 log10 copies/mL) cho thấy khả năng dự đoán chuyển đổi huyết thanh HBeAg tốt (ROC >0,75, P <0,001). Điểm cắt pgRNA >5,50 log10 copies/mL xác định được 30% người không đáp ứng ở tuần 12 (NPV >90%).
• Trong quá trình điều trị với NAs ở bệnh nhân CHB, nồng độ pgRNA huyết thanh có thể cung cấp thông tin tham khảo cho sự theo dõi lâm sàng nồng độ cccDNA trong gan, dự đoán đáp ứng của virus (VR), dự đoán chuyển đổi huyết thanh HBeAg (pgRNA <5,40 log10 copies/mL) và lựa chọn thời điểm thích hợp để ngừng điều trị kháng virus một cách an toàn, đặc biệt là khi nồng độ HBV DNA dưới ngưỡng phát hiện.
*
Serum HBV pregenomic RNA (HBV pgRNA): a new marker for the intrahepatic cccDNA activity in patients with chronic hepatitis B
Luat Nghiem Nguyen
MEDLATEC General Hospital
Tóm tắt
1) Pregenomic RNA (HBV pgRNA) is a direct transcription product of hepatitis B virus (HBV) covalently closed circular DNA (cccDNA), and it plays important roles in viral genome amplification and replication. Unlike serum HBsAg, 3.5-kb serum pgRNA is produced only from cccDNA, therefore, it can accurately reflect the transcriptional status of HBV cccDNA in the nucleus of hepatocytes.
2) Uses: HBV pgRNA can be used to predict CHB natural history, assess the response to treatment of PEG-IFN or nucleos(t)ide analogues (NAs), the seroconversion ability of HBeAg, predicts reactivation of HBV, and predicts appropriate timing for discontinuing antiviral therapy.
3) Indications: HBV pgRNA may be indicated to predict CHB natural history, assess the response to treatment of PEG-IFN or nucleos(t)ide analogues (NAs), the seroconversion ability of HBeAg, predicts reactivation of HBV, and predicts appropriate timing for discontinuing antiviral therapy. Real-time quantitative PCR to detect serum pgRNA level.
4) Serum HBV pgRNA level was measured by a real-time quantitative qPCR method with a linear range of the plasmid standard was ∼1×101 to 1×103 copies/mL and a detection limit of 1×103 copies/mL. Serum HBV pgRNA could be detected even when the serum HBV DNA level was below 20 IU/mL.
5) Clinical significance of HBV pgRNA:
• Serum HBV pgRNA can act as a biomarker to predict the phases of the natural history of disease in chronic hepatitis B patients. Serum HBV pgRNA levels were significantly lower in the HBeAg-negative patients compared to those in the HBeAg-positive patients, with the lowest levels seen in inactive carriers.
• During peginterferon alfa-2a treatment in CHB patients, serum HBV pgRNA level at treatment weeks 12 and 24 (≤5.47 and ≤5.46 log10 copies/mL, respectively) showed good ability to predict HBeAg seroconversion (ROC >0.75, P <0.001). A pgRNA cut-off of >5.50 log10 copies/mL identified 30% of nonresponders at week 12 (NPV >90%).
• During NA treatment in CHB patients, serum pgRNA level may provide a reference for clinical monitoring of intrahepatic cccDNA levels, predicts the virus response (VR), HBeAg seroconversion (HBV pgRNA <5,40 log10 copies/mL) and the selection of appropriate timing for safe discontinuing antiviral therapy, especially when HBV DNA levels are below the detection limit.
*
Viêm gan B mạn (chronic hepatitis B: CHB) hiện đang ảnh hưởng đến khoảng 260 triệu người trên thế giới, với khoảng 15-40% phát triển thành xơ gan (cirrhosis) hoặc ung thư biểu mô tế bào gan (hepatocellular carcinoma: HCC). Mặc dù việc tiêm vaccin viêm gan B có hiệu quả nhưng CHB vẫn còn là một vấn đề sức khỏe quan trọng trên toàn thế giới với nguy cơ tử vong cao. Ở bệnh nhân bị viêm gan B mạn, HBV không thể dễ dàng được loại bỏ khỏi gan, bởi vì DNA vòng giãn (relaxed circular DNA: rcDNA) được chuyển đổi liên tục thành dạng DNA vòng kín cộng hóa trị (covalently closed circular DNA: cccDNA) bền vững trong nhân tế bào gan và dạng HBV DNA tích hợp (HBV DNA integration) là dạng gắn chặt vào bộ gen trong nhân của tế bào gan. Mục tiêu việc quản lý HBV là đạt được sự ức chế virus cao, làm giảm nguy cơ của các biến chứng. Mặc dù sinh thiết gan là kỹ thuật chính xác nhất để định lượng DNA cccDNA và HBV DNA toàn phần (HBV total DNA: HBV tDNA) trong gan, nhưng đây là những kỹ thuật xâm lấn nên ít được sử dụng. Vì vậy, một số dấu ấn sinh học huyết thanh thay thế cccDNA như HBV DNA, qHBsAg và HBcrAg đã được sử dụng để đánh giá hoạt động phiên mã của HBV trong gan. Gần đây, RNA tiền gen của virus viêm gan B (HBV pregenomic RNA: HBV pgRNA), một chất trung gian của quá trình phiên mã HBV từ HBV cccDNA trong gan đã được sử dụng để theo dõi tiến trình của bệnh, đánh giá hiệu quả điều trị viêm gan B mạn.
1. Sinh học của HBV pgRNA
1.2. HBV pgRNA là gì?
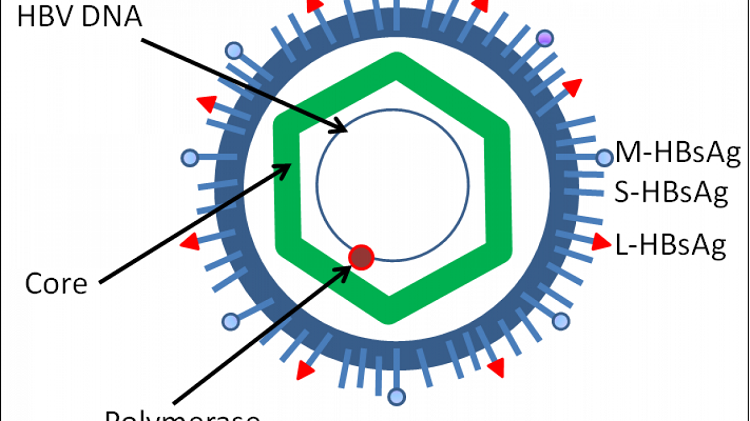
RNA tiền gen (pgRNA) là sản phẩm phiên mã trực tiếp (direct transcription product) của DNA vòng kín cộng hóa trị (covalently closed circular DNA: cccDNA) của virus viêm gan B, đóng vai trò quan trọng trong quá trình khuếch đại (amplification) và sao chép (replication) bộ gen của virus. Pregenome RNA (pgRNA) là sản phẩm phiên mã trực tiếp của cccDNA, và pgRNA có thể bị enzym HBV DNA polymerase phiên mã ngược thành rcDNA để lại tiếp tục một chu kỳ sống mới. Do đó, việc ngăn chặn phiên mã ngược sẽ không làm ảnh hưởng đến việc tạo ra pgRNA vào huyết thanh (Luo H, 2019 [8]). Khác với HBsAg huyết thanh, pgRNA huyết thanh khối lượng phân tử 3,5 kb chỉ được sản xuất từ cccDNA, do đó, nó có thể phản ánh chính xác tình trạng phiên mã (transcriptional status) của HBV cccDNA trong nhân tế bào gan (Giersch K, 2017 [3]).
1.3. Sự tạo thành HBV pgRNA
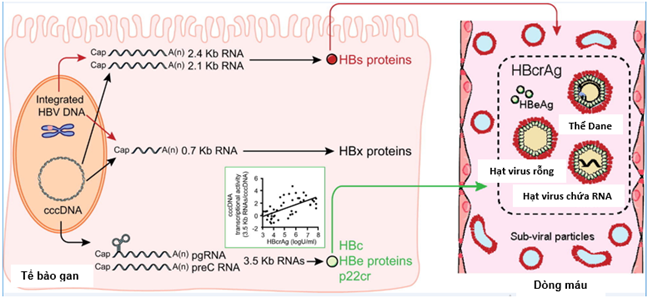
HBV dưới dạng các hạt Dane xâm nhập vào tế bào gan bằng cách gắn vào vỏ virion nhờ một số yếu tố đặc hiệu trên bề mặt tế bào gan. Màng HBV hòa màng với màng tế bào gan để xâm nhập vào tế bào gan. Vào tế bào gan, HBV trút bỏ lớp vỏ và vào nhân dưới dạng DNA vòng hở (relaxed circular DNA: rcDNA). rcDNA được chuyển đổi thành DNA dạng vòng kín cộng hóa trị (cccDNA) nhờ enzym DNA polymerase của virus. CccDNA đóng vai trò như một khuôn mẫu phiên mã cho tất cả các bản sao của virus, bao gồm 3,5kb mRNA trước lõi (precore mRNA: pcRNA) và 3,5kb RNA tiền gen (pregenomic RNA: pgRNA), các 2,4kb và 2,1kb mRNA bề mặt (surface mRNAs) và 0,7kb X mRNA (8). PgRNA là khuôn mẫu cho cả phiên mã ngược và dịch mã của enzym polymerase của virus (pol) và các protein lõi (Liu S, 2019 [6]) (Hình 1).
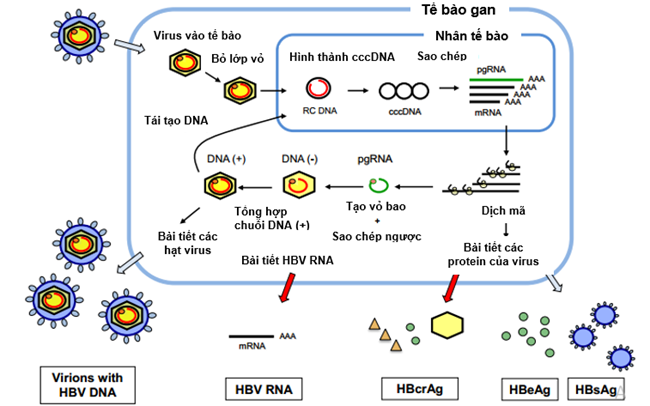
Hình 1. Sự sinh tổng hợp HBV pgRNA từ các RNA 3,5 Kb, sản phẩm của sự phiên mã của HBV cccDNA trong tế bào gan bị nhiễm HBV (Nguồn: Ganem D, et al. N Engl J Med 2004; 350 (11): 1118-1129).
2. Sử dụng HBVpgRNA
HBV pgRNA có thể được sử dụng để dự đoán các giai đoạn diễn biến tự nhiên của viêm gan B mạn (CHB), đánh giá đáp ứng với điều trị với PEG-IFN hoặc với các chất tương tự nucleos(t)ide (NAs), khả năng chuyển đổi huyết thanh của HBeAg, dự đoán sự tái hoạt động của HBV và thời điểm thích hợp để tạm dừng điều trị kháng virus.
3. Chỉ định
HBV pgRNA có thể được chỉ định để dự đoán các giai đoạn diễn biến tự nhiên của viêm gan B mạn (CHB), đánh giá đáp ứng với điều trị PEG-IFN hoặc các chất tương tự nucleos(t)ide (NAs), sự chuyển đổi huyết thanh của HBeAg, dự đoán sự tái hoạt động của HBV và thời điểm thích hợp để tạm ngừng điều trị kháng virus.
4. Định lượng HBV pgRNA huyết thanh
Nồng độ pgRNA của HBV huyết thanh có thể được phát hiện bằng phản ứng chuỗi polymerase định lượng thời gian thực (real-time quantitative polymerase chain reaction qPCR) trong hệ thống phát hiện PCR thời gian thực LightCycler 480 II (Roche, Mannheim, Đức) với phương pháp thăm dò SYBR Green hoặc TaqMan®. Các đoạn nucleotide mồi đặc hiệu (specific primers) và đầu dò (TaqMan probe) được sử dụng để phát hiện HBV 3,5 kb RNA như sau:
Mồi xuôi (forward primer): 5′-AYAGACCATCAAATGCCC-3 ′;
Mồi ngược (reverse primer): 5′-ATTCTCAGACCGTAGCACACGACAC-3 ′ và
Đầu dò (probe): 5′-CTTATCAACACTTCCGGARACTACTGTTGTTAGAC-BHQ1-3′.
Nồng độ pgRNA của HBV huyết thanh được đo bằng phương pháp qPCR định lượng thời gian thực với phạm vi tuyến tính của plasmid tiêu chuẩn là ∼1×101 đến 1×103 copies/mL và giới hạn phát hiện là 1×103 copies/mL. HBV PgRNA huyết thanh có thể được phát hiện ngay cả khi mức độ HBV DNA trong huyết thanh dưới 20 IU/mL (Lin N, 2020 [5]).
5. Ý nghĩa lâm sàng của HBV pgRNA
5.1. Giá trị của HBV pgRNA trong đánh giá lịch sử tự nhiên của nhiễm HBV mạn
5.1.1. HBV pgRNA dự đoán các giai đoạn trong diễn biến tự nhiên của nhiễm HBV mạn
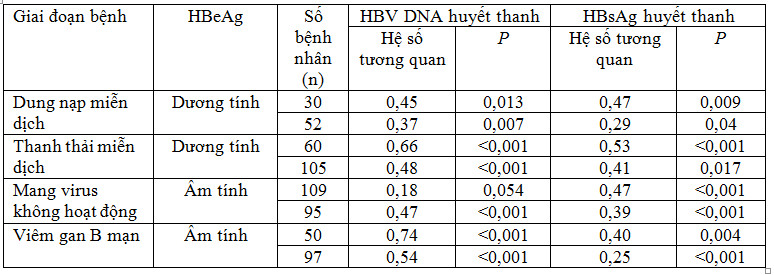
Trong diễn biến tự nhiên của nhiễm HBV mạn, có sự khác biệt rất rõ rệt về giá trị HBV pgRNA huyết thanh giữa các bệnh nhân ở các giai đoạn (phases) khác nhau (dung nạp miễn dịch = 7,87, phản ứng miễn dịch = 6,67, mang virus không hoạt động = 2,00 và viêm gan mạn HBeAg âm tính = 5,31 copies/mL). Nhóm mang virus không hoạt động có giá trị HBV RNA huyết thanh thấp nhất so với những nhóm khác và giá trị này thấp hơn rất rõ rệt so với giá trị của giai đoạn viêm gan HBeAg âm tính. Giá trị trung bình của các dấu ấn sinh học trong các gia đoạn nhiễm HBV mạn được thể hiện ở Bảng 1.
Bảng 1. Giá trị trung bình của các dấu ấn sinh học trong các gia đoạn nhiễm HBV mạn (Liu Y, 2019 [7]).
5.1.2. HBV pgRNA dự đoán sự tái hoạt động ở bệnh nhân viêm gan B mạn HBeAg âm tính
Mặc dù nồng độ HBV pgRNA có xu hướng giảm khi chuyển đổi huyết thanh thành HBeAg âm tính và không hoạt động, nhưng những nồng độ này sẽ tăng lên nếu có sự tái hoạt động thành dạng viêm gan hoạt động. Liu Y và cộng sự, 2019 [7] đã đánh giá tác dụng tiềm năng của HBV pgRNA huyết thanh để phân biệt bệnh nhân “mang HBV không hoạt động” (inactive carrier) và “viêm gan B mạn HBeAg âm tính” (HBeAg-negative hepatitis B). Nồng độ HBV pgRNA huyết thanh ở ngưỡng >2,11 log copies/mL cho phép dự đoán giai đoạn viêm gan mạn HBeAg âm tính với độ chính xác 78,19%, độ nhạy 84,21%, độ đặc hiệu 73,68%, giá trị dự đoán dương tính (PPV) 70,59%, giá trị dự đoán âm tính (NPV) 86,15% và độ chính xác là 78,19%. Ngoài ra, nồng độ HBV pgRNA huyết thanh cũng cho thấy sự vượt trội rõ ràng của sự kết hợp của HBV DNA huyết thanh (ngưỡng >3,39 log copies/mL) và HBsAg (ngưỡng >2,74log IU/mL) trong việc phân biệt hai giai đoạn này của nhiễm HBV mạn HBeAg âm tính (Bảng 2).
Bảng 2. Nồng độ HBV pgRNA dự đoán tái hoạt động của nhiễm HBV mạn tính HBeAg âm tính (Liu Y, 2019 [7]).
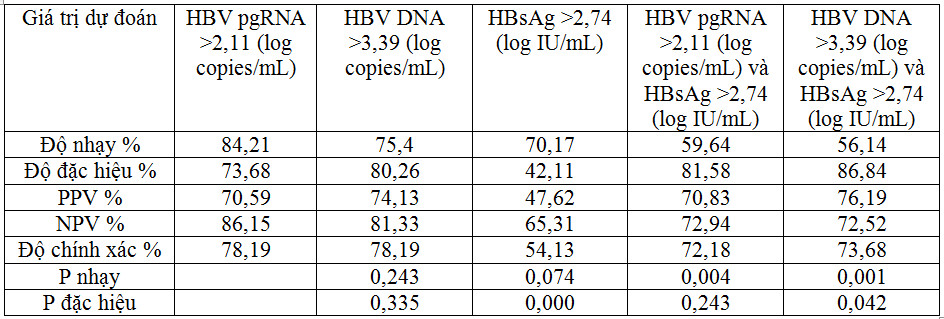
Ghi chú: PPV giá trị dự đoán dương tính, 70,59%, NPV: giá trị dự đoán âm tính, P nhạy: sác xuất so sánh độ nhạy của HBV pgRNA với các dấu ấn khác, P đặc hiệu: sác xuất so sánh độ đặc hiệu của HBV pgRNA với các dấu ấn khác.
5.2. Giá trị của HBV pgRNA trong theo dõi điều trị bằng thuốc kháng virus
Hiện nay, các loại thuốc được chấp thuận để điều trị viêm gan B mạn trên thế giới gồm 2 thuốc để tiêm dưới da là inteferon α-2a và peginteferon α-2a, là các thuốc điều biến miễn dịch và 5 loại thuốc uống tương tự nucleos(t)ide (NAs), là các thuốc ức chế enzym phiên mã ngược của virus (viral reverse transcriptase), trong đó có 3 thuốc tương tự nucleoside là lamivudine (LAM), telbivudine (LdT), entecavir (ETV), và 2 thuốc tương tự nucleotide mạch hở là adefovir dipivoxil (ADV) và tenofovir disoproxil fumarate (TDF). Nồng độ HBV pgRNA huyết thanh có thể giúp dự đoán đáp ứng của virus (VR), sự chuyển đổi huyết thanh HBeAg và lựa chọn thời điểm thích hợp để dừng điều trị kháng virus một cách an toàn, đặc biệt là khi nồng độ HBV DNA dưới ngưỡng phát hiện.
5.2.1. Giá trị của HBV pgRNA trong đánh giá đáp ứng điều trị với peginterferon (peg-IFN)
HBV RNA huyết thanh có thể là một dấu ấn dự báo cho đáp ứng peginterferon Alfa-2a ở bệnh nhân viêm gan B mạn HBeAg dương tính (HBeAg-positive chronic hepatitis B). RNA của virus viêm gan B (HBV) là một dấu ấn sinh học huyết thanh mới có khả năng dự đoán đáp ứng điều trị ở bệnh nhân viêm gan B. Trong một nghiên cứu trên 131 đối tượng (70% nam, 96% người châu Á, 35% HBV kiểu gen B và 61% C), 76 người được điều trị bằng peginterferon alfa-2a một mình và 55 người được điều trị bằng peginterferon alfa-2a kết hợp với lamivudine, Bömmel FV và cộng sự, 2018 [1] thấy rằng nồng độ RNA HBV trung bình thấp hơn đáng kể, tại mọi thời điểm, ở những bệnh nhân đạt được chuyển đổi huyết thanh HBeAg. Nồng độ HBV RNA ở tuần điều trị 12 và 24 cho thấy khả năng dự đoán tốt sự chuyển đổi huyết thanh HBeAg (diện tích vùng dưới đường cong ROC >0,75, P <0,001). Điểm cắt HBV RNA >5,50 log10 copies/mL xác định được 30% người không đáp ứng ở tuần 12 (với NPV >90%).
Trong một nghiên cứu khác trên 727 bệnh nhân có HBeAg dương tính với điều trị PegIFNα-2a hoặc PegIFNα-2b trong 48 tuần và theo dõi không điều trị trong 24 tuần, Zhang M và cộng sự, 2020 [12] cũng thấy rằng, ở tuần điều trị thứ 72, sự chuyển đổi huyết thanh HBeAg được thấy ở 217 bệnh nhân (29,8%) và sự mất HBsAg được thấy ở 21 bệnh nhân (2,9%). Trong quá trình điều trị 48 tuần, HBV RNA giảm nhanh hơn HBV DNA và HBsAg. Giá trị cắt tối ưu của HBV pgRNA để đánh giá đáp ứng điều trị PFN ở tuần thứ 12 là ≤5,47 copies/mL (tương ứng với độ nhạy, độ đặc hiệu, PPV, NPV và ROC là 97, 30, 59, 92 và 0,77). Giá trị cắt tối ưu của HBV pgRNA để đánh giá đáp ứng điều trị PFN ở tuần thứ 24 là ≤5,26 copies/mL (tương ứng với độ nhạy, độ đặc hiệu, PPV, NPV và ROC là 97, 24, 58, 90 và 0,82). Ở tuần điều trị viêm gan B mạn bằng PFN thứ 12, giá trị cắt của HBV pgRNA để đánh giá bệnh nhân không đáp ứng (nonresponsers) là ≥5,50 log copies/mL với tỷ lệ không đáp ứng là 30% và ở tuần thứ 24, giá trị cắt của HBV pgRNA để đánh giá bệnh nhân không đáp ứng là ≥5,70 log copies/mL với tỷ lệ bệnh nhân không đáp ứng là 24%.
Như vậy, HBV RNA có thể là dấu ấn theo dõi hiệu quả đáp ứng điều trị và dự đoán chuyển đổi huyết thanh HBeAg ở bệnh nhân HBeAg dương tính được điều trị bằng pegylated interferon.
5.2.2. Đánh giá đáp ứng điều trị đối với các thuốc kháng virus tương tự nucleot(s)ide (NA)
Về giá trị của HBV pgRNA trong huyết thanh trong đánh giá đáp ứng điều trị đối với các thuốc kháng virus tương tự nucleot(s)ide (NA), là một kỹ thuật không xâm lấn, việc đo nồng độ HBV pgRNA huyết thanh có thể đóng vai trò là dấu ấn sinh học huyết thanh mới trong điều trị, theo dõi và tiên lượng nhiễm HBV.
Trong một nghiên cứu Yu X và cộng sự, 2019 [11] thấy rằng nồng độ HBV pgRNA huyết thanh ban đầu tương quan mạnh với nồng độ HBV DNA (r = 0,82, p <0,001), tương quan vừa với nồng độ HBsAg (r = 0,69, p <0,001) và tương quan yếu với alanine aminotransferase (ALT) huyết thanh (r = 0,28, p <0,05). Các bệnh nhân được điều trị với ETV có sự chuyển đổi huyết thanh HBeAg cho thấy nồng độ pgRNA HBV huyết thanh giảm mạnh hơn ở các tuần điều trị thứ 4, 12, 24 và 48. Lúc đầu, diện tích dưới đường cong ROC (AUC) của HBV pgRNA là 0,68, tương quan với HBV DNA (AUC = 0,66 ) và HBsAg (AUC = 0,64) ở bệnh nhân điều trị ETV. Trong quá trình điều trị, dự đoán tốt nhất về chuyển đổi huyết thanh HBeAg ở bệnh nhân điều trị với ETV là nồng độ HBV pgRNA huyết thanh ở tuần thứ 4 (AUC = 0,71, với giá trị cắt, độ nhạy, độ đặc hiệu, PPV và NPV tương ứng là 7,95 log10 copies/mL, 83%, 56%, 40%, 91%).
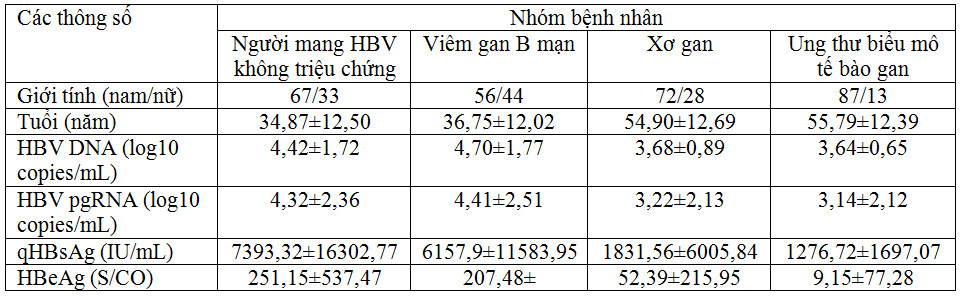
Trong một nghiên cứu khác trên 400 bệnh nhân viêm gan B mạn, gồm 4 nhóm: nhóm người mang HBV không triệu chứng (asymptomatic hepatitis B virus carrier: ASC), viêm gan B mạn (chronic hepatitis B: CHB), xơ gan (liver cirrhosis: LC) và ung thư biểu mô tế bào gan (hepatocellular carcinoma: HCC), mỗi nhóm gồm 100 bệnh nhân, Lin N và cộng sự, 2020 [5] thu được các kết quả như được chỉ ra ở Bảng 3.
Bảng 3. Sự thay đổi về một số thông số sinh học trong các tình trạng lâm sàng của viêm gan B mạn (Lin N, 2020 [5]).
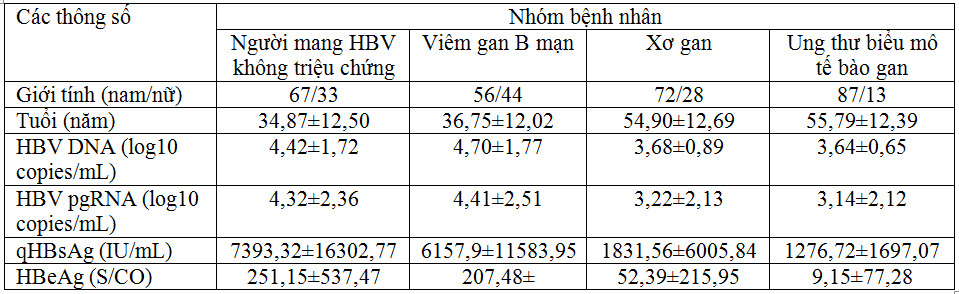
Sự khác biệt rất rõ rệt về nồng độ HBV pgRNA, HBV DNA và HBsAg giữa các nhóm người mang HBV không triệu chứng (ASC), viêm gan B mạn (CHB), xơ gan (LC) và ung thư biểu mô tế bào gan được chỉ ra ở Hình 2.
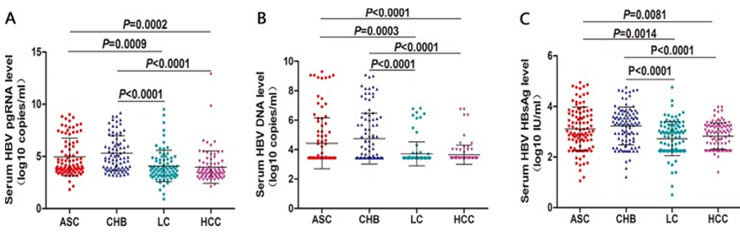
Hình 2. So sánh nồng độ HBV pgRNA, HBV DNA, và HBsAg huyết thanh ở 4 nhóm bệnh nhân nhiễm HBV khác nhau, mỗi nhóm n=100. (A) nồng độ HBV pgRNA, (B) HBV DNA (B) và (C) HBV HBsAg (Lin N, 2020 [5]).
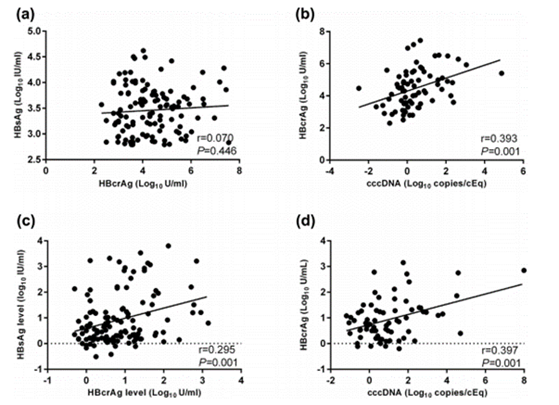
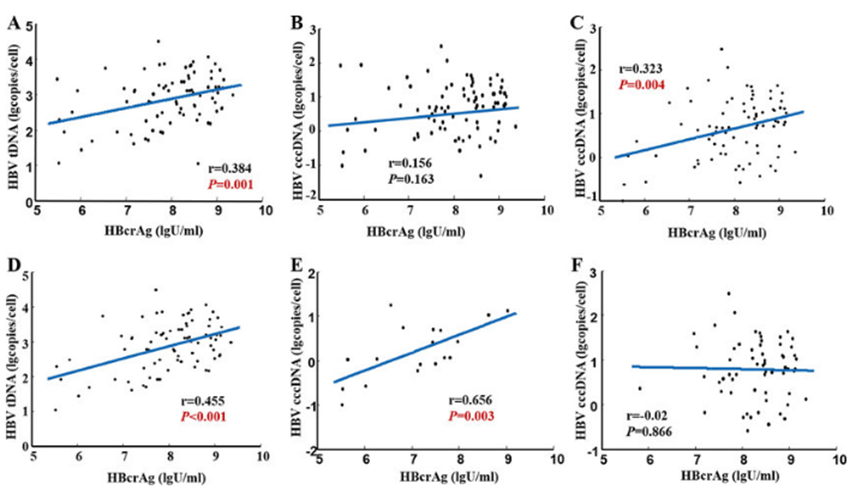
Các tác giả cũng thấy có sự tương quan rất rõ rệt giữa nồng độ HBV pgRNA với HBsAg và với HBV DNA huyết thanh ở bệnh nhân nhiễm HBV (Hình 3).
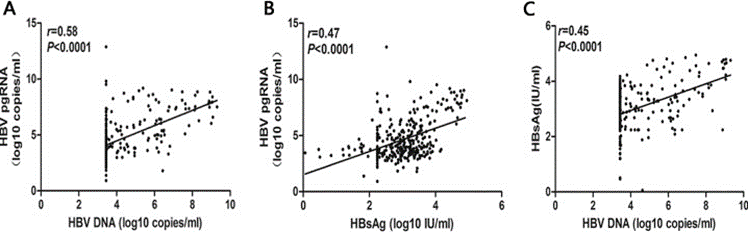
Hình 3. Sự tương quan giữa nồng độ HBV pgRNA với HBsAg và với HBV DNA huyết thanh ở bệnh nhân nhiễm HBV(Lin N, 2020 [5]) .
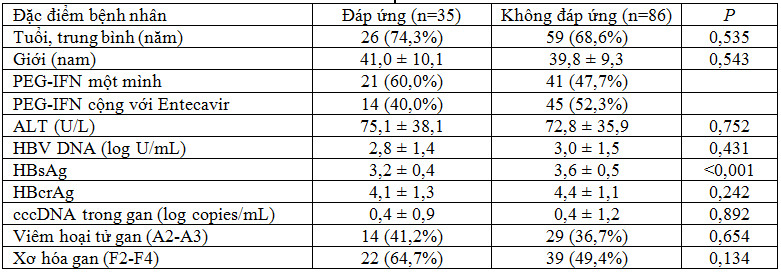
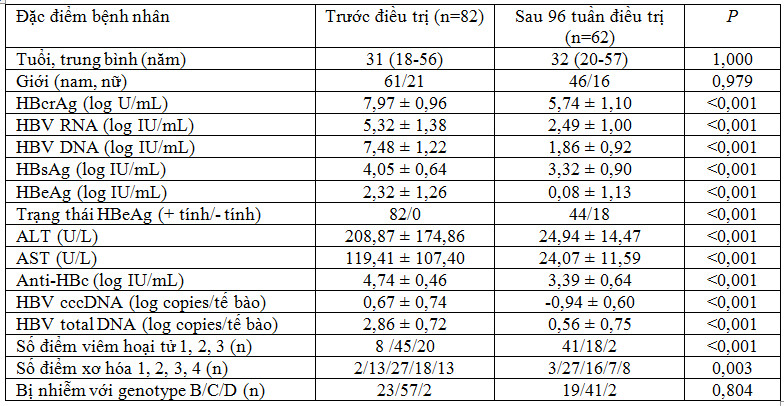
Các tác giả còn thấy rằng tỷ lệ phát hiện HBV pgRNA trong các mẫu huyết thanh có nồng độ HBV DNA <500 IU/mL là 78,9%, và tỷ lệ không phát hiện được là 21,1%. Dựa trên kết quả này, các tác giả đã chọn các bệnh phẩm từ 108 bệnh nhân nhiễm HBV HBeAg âm tính để phân tích thêm, gồm 74 bệnh phẩm có nồng độ HBV DNA <20 IU/mL và 34 bệnh phẩm có nồng độ HBV DNA > 20 IU/mL nhưng <500 IU/mL. Phân tích thống kê cho thấy tỷ lệ phát hiện HBV pgRNA ở cả hai nhóm lần lượt là 17,57% (13/74) và 41,18% (14/34). Tỷ lệ HBV pgRNA không phát hiện được ở cả hai nhóm lần lượt là 82,43% (61/74) và 58,82% (20/34) (Bảng 4).
Bảng 4. Đặc điểm lâm sàng và xét nghiệm của bệnh nhân có nồng độ HBV DNA <500 IU/mL (Lin N, 2020 [5]).
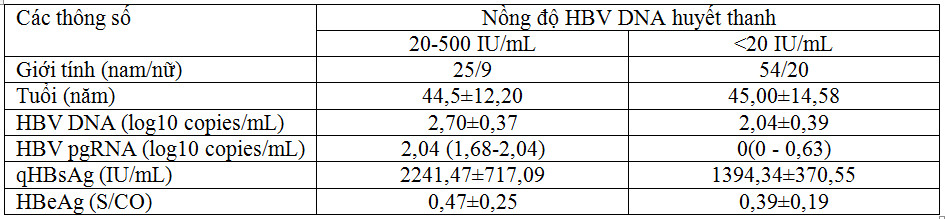
Ghi chú: HBV DNA 1 IU/mL=5,60 copies/mL; S/CO=sample/cut-off (giá trị mẫu đo/giá trị cắt).
Về sự tương quan của HBV pgRNA huyết thanh với nồng độ HBV cccDNA trong gan, sau 96 tuần điều trị với NAs, sự giảm của HBV pgRNA huyết thanh tương quan rõ rệt với sự giảm của HBV cccDNA trong gan (r = 0,765, P <0,001) (Wang L, 2019 [9]).
Về giá trị cắt của HBV pgRNA để dự đoán chuyển đổi huyết thanh HBeAg, Wang X và cộng sự, 2020 [10] thấy rằng, giá trị ngưỡng để chuyển đổi huyết thanh HBeAg ở tuần 24 của HBV pgRNA là 250.000 copies/mL (5,40 log10 copies/mL) với độ nhạy là 57,6%, độ đặc hiệu là 79,5% và độ chính xác cao (78,3%). Những bệnh nhân có giá trị HBV pgRNA <5,40 log10 copies/mL có 72,73% chuyển đổi huyết thanh HBeAg. Sự kết hợp của HBV pgRNA với HBeAg ở tuần thứ 24 mang lại hiệu quả tốt hơn so với HBV RNA đơn lẻ. AUROC của sự kết hợp tăng lên 0,821 (△ AUROC = 0,067, P = 0,02), và độ chính xác tăng lên 86,49%. Các bệnh nhân có HBV pgRNA <5,40 log10 copies/mL và HBeAg <20 S/CO có 95,83% chuyển đổi huyết thanh HBeAg. Như vậy, sự kết hợp của HBV pgRNA và HBeAg ở tuần thứ 24 có thể cho dự đoán cao hơn về đáp ứng điều trị.
Về giá trị của HBV pgRNA trong dự đoán khả năng dừng điều trị một cách an toàn ở bệnh nhân viêm gan B mạn, Kostyusheva A và cộng sự, 2018 [4] thấy rằng, có thể dừng điều trị thuốc tương tự nucleos(t)ide một cách an toàn (safely discontinuing NA therapy) khi HBV pgRNA không có khả năng được phát hiện. Theo Ding WB và cộng sự, 2019 [2], vì HBV cccDNA không thể được loại bỏ hoàn toàn trong quá trình trị liệu NA, hầu hết bệnh nhân CHB đã bị tái phát, gây khó khăn cho việc quyết định thời điểm ngừng điều trị NA. Vì vậy, phần lớn bệnh nhân CHB cần điều trị với NAs trong một thời gian dài, thậm chí cả đời, điều này làm tăng thêm gánh nặng tài chính cho cả bệnh nhân và xã hội. Vì HBV RNA huyết thanh có thể được coi là một dấu ấn tiềm năng cho hoạt động của cccDNA, nên sự biến mất của HBV pgRNA huyết thanh có thể là một dấu ấn của sự dừng phiên mã của cccDNA. Do đó, HBV pgRNA huyết thanh có thể đóng vai trò là một dấu ấn dự đoán tiềm năng để dừng điều trị với NAs một cách an toàn.
Funadin giúp khử độc, bảo vệ gan, giúp điều trị men gan cao, gan nhiễm mỡ, phòng ngừa xơ gan, ung thư gan, viêm gan virus. Khi chúng ta sử dụng sản phẩm này thì chúng ta hoàn toàn có thể yên tâm về sức khỏe gan, thận, phổi. Dưới đây chúng ta cùng đi tìm hiểu chi tiết về sản phẩm.

Funadin là sự kết hợp giữa các thảo dược quý hiếm, các chất chống oxy hoá, khử gốc tự do và các chất dinh dưỡng đặc hiệu như albumin, globulin miễn dịch, proteins, các axit amin cần thiết được phân đoạn, chiết xuất ở cấp độ phân tử ADN từ gan tươi và gan sấy khô cung cấp đầy đủ toàn diện các chất dinh dưỡng giúp cải thiện chức năng gan, thận và phổi.
Funadin với các tinh chất dinh dưỡng hoàn toàn tự nhiên nhằm mục tiêu nuôi dưỡng, bảo vệ chức năng gan, thận và phổi, duy trì hoạt động khoẻ mạnh của các tế bào Kupffer, tế bào gan, tiểu cầu thận và làm trẻ hóa các mô chức năng, giúp phòng ngừa và cải thiện, hỗ trợ hiệu quả điều trị các bệnh lý cả gan, thận và phổi.
Funadin đã chứng tỏ được kết quả tuyệt vời khi dùng để điều trị các bệnh rối loạn về chức năng gan, thận và phổi do ô nhiễm không khí, môi trường, rượu bia, ma túy và các chất độc hại khác trong thuốc men hay thực phẩm. Đặc biệt trong hỗ trợ điều trị hội chứng gan thận, một trong những điều quan trọng của chế độ ăn uống đúng tiêu chuẩn để giữ gìn sức khỏe cho gan và thận là cung cấp đầy đủ chất đạm giúp tái tạo tế bào T, các chất khoáng interferons, globulins, đây là yếu tố để cơ thể chống nhiễm trùng.
Funadin điều hòa chuyển hóa protein bằng cách cân bằng các chức năng trao đổi chất cho gan, tuyến yên và tuyến thượng thận; giảm gánh nặng trên thận. Sử dụng Funadin hàng ngày thúc đẩy quá trình chuyển hoá thuốc, giúp giảm viêm, tăng mức năng lượng và làm trẻ hoá làn da, mịn màng, kiểm soát cân nặng, điều hoà huyết áp và tăng cường sức khoẻ xuong khớp.
* Đối tượng sử dụng Funadin: Người trưởng thành nhằm nâng cao sức khỏe gan và thận, những người bị tăng men gan, viên gan siêu vi, viêm gan cấp, mãn, gan nhiễm mỡ, suy gan, xơ gan... đang điều trị hóa chất, xạ trị hoặc các thuốc chống lao, các thuốc chữa ung thư..., viêm cầu thận cấp, mãn, suy giảm chức năng thận, suy thận cấp và mãn, hội chứng thận hư, thận nhiễm mỡ...
* Hướng dẫn sử dụng Funadin: Uống 1 viên/lần x 2 đến 3 lần/ngày, uống sau ăn hoặc uống theo hướng dẫn của bác sĩ hoặc chuyên gia y tế. Mỗi đợt điều trị từ 3 đến 6 tháng.
Chi tiết xem thêm sản phẩm tại: >>> TPCN Funadin - tăng khả năng giải độc bảo vệ gan
Tài liệu tham khảo
1. Bömmel FV, Bömmel AV, Krauel A, et al. Serum HBV RNA as a Predictor of Peginterferon Alfa-2a Response in Patients With HBeAg-Positive Chronic Hepatitis B. J Infect Dis 2018 Aug 24; 218(7): 1066-1074.
2. Ding WB, Wang MC, Zhang JN, et al. Novel insights of HBV RNA in hepatitis B virus pathogenesis and clinical application. Hepatoma Res 2019; 5: 10.
3. Giersch K, Allweiss L, Volz T, Dandri M, Lütgehetmann M. Serum HBV pgRNA as a clinical marker for cccDNA activity. J Hepatol 2017; 66(2): 460-462.
4. Kostyusheva A, Kostyushev D, Brezgin S, Volchkova E, and Chulanov V. Clinical Implications of Hepatitis B Virus RNA and Covalently Closed Circular DNA in Monitoring Patients with Chronic Hepatitis B Today with a Gaze into the Future: The Field Is Unprepared for a Sterilizing Cure. Genes (Basel) 2018 Oct; 9(10): 483.
5. Lin N, Ye A, Lin J, et al. Diagnostic Value of Detection of Pregenomic RNA in Sera of Hepatitis B Virus-Infected Patients with Different Clinical Outcomes. J Clin Microbiol 2020 Jan 28; 58(2): e01275-19.
6. Liu S, Zhou B, Valdes JD, Sun J, and Guo H. Serum HBV RNA: a New Potential Biomarker for Chronic Hepatitis B Virus Infection. Hepatology 2019 Apr; 69(4): 1816-1827.
7. Liu Y, Jiang M, Xue J, et al. Serum HBV RNA quantification: useful for monitoring natural history of chronic hepatitis B infection. BMC Gastroenterology 2019; 19(53): 72.
8. Luo H, Zhang XX, Cao LH, et al. Serum hepatitis B virus RNA is a predictor of HBeAg seroconversion and virological response with entecavir treatment in chronic hepatitis B patients. World J Gastroenterol 2019 Feb 14; 25(6): 719-728.
9. Wang L, Cao X, Wang Z, et al. Correlation of HBcrAg with Intrahepatic Hepatitis B Virus Total DNA and Covalently Closed Circular DNA in HBeAg-Positive Chronic Hepatitis B Patients. J Clin Microbiol 2019; 57(1): e01303-01318.
10. Wang X, Wang Z, Chi X, et al. Efficacy of a Combination of HBV RNA and HBeAg in Predicting HBeAg Seroconversion in Patients Treated with Entecavir for 144 Weeks. Int J Infect Dis 2020 Jul; (in press).
11. Yu X, Yu D, Gong Q, Chen P, Zhang X. Dynamic changes of serum HBV pgRNA levels in patients with chronic hepatitis B treated with entecavir or peg-interferon. J Hepatol 2019; 70(1): e490.
12. Zhang M, Li GD, Shang J, et al. Rapidly decreased HBV RNA predicts responses of pegylated interferons in HBeAg-positive patients: a longitudinal cohort study. Hepatol Int 2020 Mar; 14(2): 212-224.